
1
腎細胞癌(腎癌,Renal Cell Carcinoma,RCC)乃泌尿系統常見的癌症之一,早期的標準治療方式為手術,惟部分患者於術後仍有一定的復發風險,甚至出現擴散。以往,RCC並無經證實有效的術後輔助治療,猶幸隨著醫藥進步,近年一項第三期臨床研究證實,RCC患者在術後採用免疫治療藥物作輔助治療,能有效降低復發風險,並顯著延長患者的存活期,成為首個被美國食品藥物管理局(FDA)和歐盟核准用於經手術切除後具中高或高復發風險的RCC患者的輔助治療。
撰文:泌尿外科專科醫生 黃俊謙醫生
為什麼術後仍需要「輔助」治療?
RCC與所有其他癌症一樣,即使腫瘤已被完全切除,癌症仍有機會復發,而具有高風險特徵的患者,復發機會更高。手術旨在切除肉眼可見的腫瘤,但可能無法清除所有癌細胞。輔助治療是為了進一步消滅那些未被肉眼看得到的微小殘留癌細胞,避免它們他日伺機而動,東山再起。另一方面,部分個案在切除原發腫瘤之前,癌細胞可能已經轉移至身體其他部位,輔助治療可清除這些未被影像檢測到的微小擴散,從而降低復發或擴散的風險。
輔助治療突破-免疫檢查點抑制劑
昔日,RCC並無經證實有效降低復發風險和改善存活期的術後輔助治療,原因是RCC對傳統化療和放射治療反應並不理想。醫學界曾對應用於晚期或轉移性RCC的標靶藥物「酪胺酸激酶抑制劑」(Tyrosine Kinase Inhibitor,TKI)進行研究,以評估其作為RCC術後輔助治療的臨床效益,惟不同的研究結果出現矛盾,其中一項薈萃分析表明該TKI無法改善患者的整體存活率。此外,該TKI的藥物副作用較大,影響患者的生活質素,不少患者因而需要停藥。
幸而,近年在腫瘤領域嶄露頭角的免疫治療為RCC術後輔助治療帶來突破。免疫治療已陸續被應用於各種癌症,而其中一款免疫檢查點PD-1抑制劑的免疫治療藥物,已被證實有效降低術後RCC患者的復發風險和死亡率。
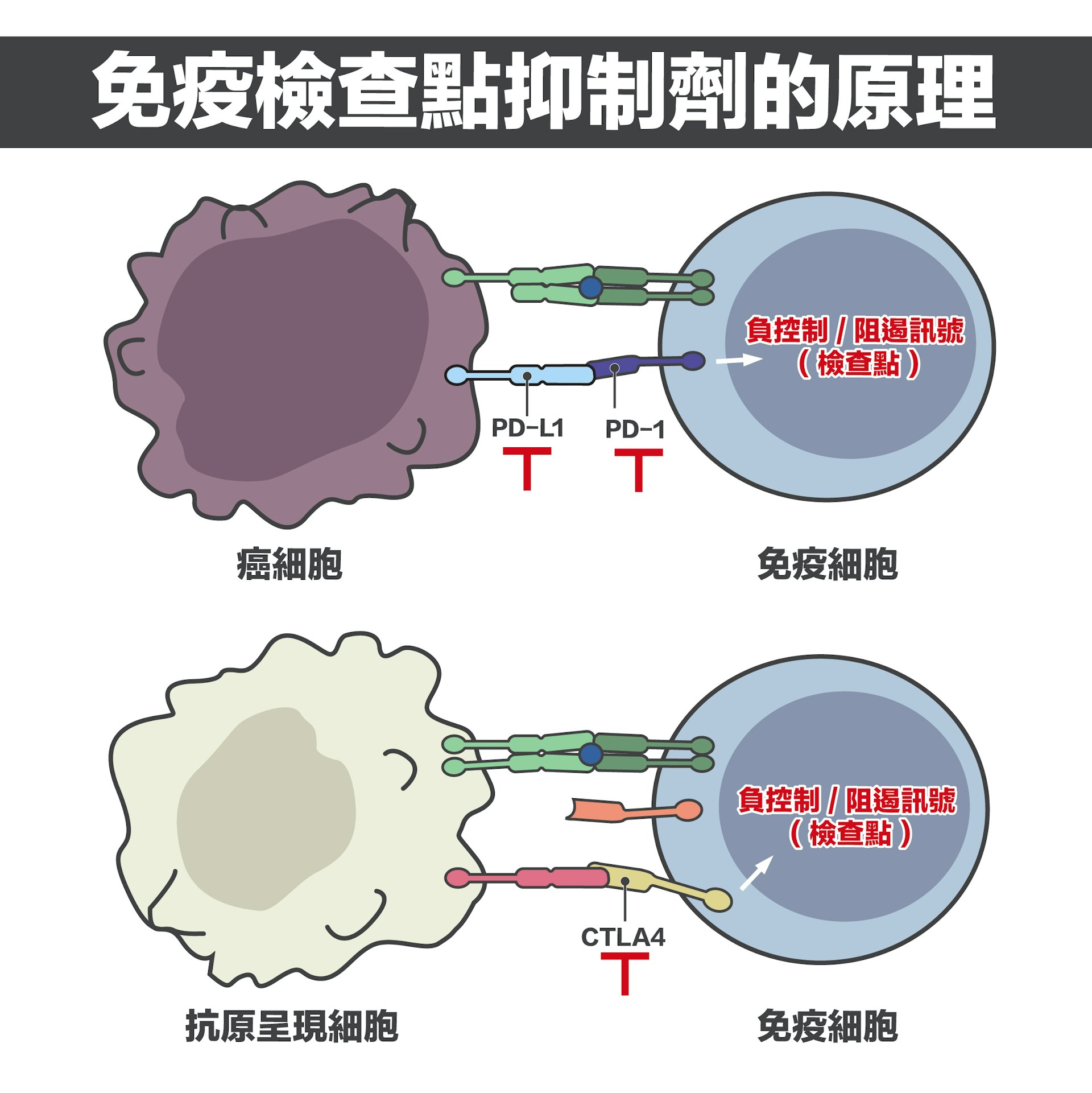
免疫檢查點抑制劑(Checkpoint Inhibitor)的原理
人體免疫系統具自我保護機制,此機制好比出境過關必經的「檢查點」(checkpoint),當偵測出外來入侵者或不屬於自身的物質時,例如細菌、病毒和癌細胞,便會啟動免疫反應將其驅趕或殲滅。然而,狡猾的癌細胞懂得「偽裝」──癌細胞和免疫細胞表面均存在一些蛋白質,當兩者的某些蛋白質連結,免疫系統的功能便會被剎停,因而無法辨識出癌細胞並將之消滅。情況好比癌細胞上的PD-L1蛋白向免疫細胞上的PD-1蛋白伸出「友誼之手」,當兩手一握,免疫系統便會誤以為癌細胞是「朋友」,任由其留在體內繼續生長。免疫治療就是利用藥物將癌細胞的偽裝面具撕破,重新啟動免疫系統辨識和攻擊癌細胞的功能。
該款免疫檢查點PD-1抑制劑在一項第三期臨床研究中被證實用於高復發風險的RCC患者作為術後輔助治療,復發風險降低了28%,整體死亡率降低了38%。在術後第48個月,曾接受PD-1抑制劑輔助治療療程的患者僅有9%死亡,而未接受該藥的患者則有14%死亡。相對於傳統標靶藥物TKI,PD-1抑制劑的副作用較小,患者的生活質素和對治療的耐受性更理想,出現嚴重副作用並因而需要停藥的機會也較低。基於這項研究結果,美國FDA和歐盟等已核准該PD-1抑制劑應用於經手術切除後具中高或高復發風險的RCC患者的輔助治療。
這項研究結果無疑為RCC術後輔助治療開闢了新蹊徑,令人鼓舞。建議RCC患者在術後向您的泌尿外科醫生或腫瘤科醫生查詢,以評估PD-1抑制劑能否為您帶來臨床效益。
知多一點點
問:哪些RCC患者術後具有高復發風險,可考慮使用術後輔助免疫治療?
答:要評估復發風險高低,癌症的TNM分期(即腫瘤的大小、是否有淋巴結或遠端轉移)和腫瘤的惡性程度均為關鍵。上述研究結果分別在2021年和2024年發表於《新英格蘭醫學期刊》(New England Journal of Medicine)上,指出若腎癌細胞屬於透明細胞(clear cell RCC),且具有以下高復發風險特徵的患者,有機會可受益於術後輔助免疫治療:
•TNM分期屬於第II期,腫瘤惡性程度第四級(pT2G4);或
•TNM分期屬於第II期,以及伴有肉瘤樣變化(sarcomatoid);或
•TNM分期屬於第III或第IV期(pT3 / pT4);或
•出現局部淋巴結轉移(N1);或
•癌細胞已經轉移,但原發和所有轉移腫瘤均已被切除(M1)。

泌尿外科專科醫生 黃俊謙醫生
